DNA和RNA是细胞内两类关键生物大分子,在基因表达调控和蛋白质合成等生命过程中发挥核心作用。然而,在内源性代谢压力及外源环境应激条件下,二者均可能发生损伤。过去几十年,DNA损伤应答与修复网络因其在疾病发生及肿瘤治疗中的重要作用而得到系统研究。与此同时,越来越多证据表明,多数化疗药物具有多靶点效应,在诱导DNA损伤的同时亦可引发RNA损伤。相比之下,RNA损伤及其应答机制在化疗过程中的作用仍缺乏系统性认识。
近日,香港色情片
基础医学院赵书博副教授联合德国慕尼黑大学Julian Stingele教授团队和剑桥大学Stephen P. Jackson教授团队在分子生物学领域顶级期刊Molecular Cell 发表了题为 RNF25 confers mRNA damage tolerance by curbing activation of the integrated stress response 的研究论文。该研究首次揭示了RNA损伤诱导的整合应激反应(Integrated Stress Response, ISR)在急性髓系白血病化疗药物阿扎胞苷作用过程中的关键作用,并系统阐明了泛素连接酶RNF25介导细胞抵抗药物细胞毒性的分子机制,突破了阿扎胞苷“主要通过损伤DNA发挥作用”的传统认知。该工作得到了香港色情片
“培英”计划的资助。
传统研究认为,阿扎胞苷作为核苷类似物主要通过掺入DNA发挥低甲基化及DNA损伤作用。然而,在体内约80%–90%的阿扎胞苷实际掺入RNA,提示RNA可能是其关键作用靶点之一。围绕这一问题,作者基于胞苷与脱氧胞苷在细胞内代谢通路的差异,构建了阿扎胞苷与地西他滨的对照分析体系,并结合全基因组CRISPR/Cas9筛选,系统绘制了阿扎胞苷作用机制的调控图谱,从而深化了对其分子机制的整体认知。研究进一步发现,RNF25是调控阿扎胞苷敏感性的关键因子;结合泛素化蛋白质组学分析,鉴定核糖体蛋白eS31第113位赖氨酸为RNF25的关键作用位点。
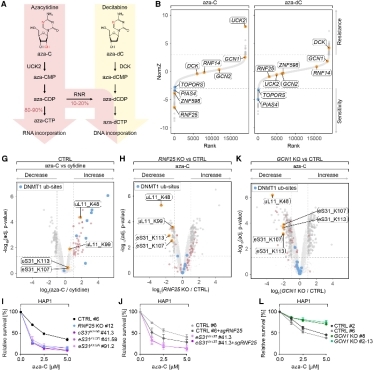
图1:RNF25通过泛素化eS31发挥抵抗阿扎胞苷细胞毒性的保护作用
作者进一步通过磷酸化蛋白质组学分析发现,阿扎胞苷可特异性激活整合应激反应(ISR)。功能分析表明,ISR的激活是其细胞毒性的主要来源。结合核糖体印迹分析与点击化学实验,研究揭示阿扎胞苷掺入mRNA后发生化学结构改变,进而导致核糖体翻译停滞与碰撞,激活GCN2依赖的ISR通路,引发翻译抑制及细胞毒性。进一步研究表明,RNF25介导的eS31泛素化修饰可抑制ISR的过度激活,从而减轻阿扎胞苷的细胞毒性作用。
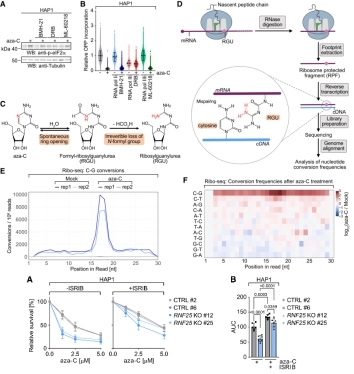
图2:阿扎胞苷掺入mRNA后激活整合应激反应并介导细胞毒性
综上,该研究首次证实阿扎胞苷可通过诱导mRNA损伤并ISR发挥细胞毒性作用,同时揭示RNF25通过调控该应激通路介导细胞对阿扎胞苷毒性的抵抗机制,提出了一条新的mRNA损伤耐受调控通路。该成果不仅深化了对阿扎胞苷作用机制的认识,也表明化疗药物疗效与RNA损伤应答密切相关。相关发现为通过靶向RNA损伤应答通路以提高化疗疗效、降低毒副作用提供了重要理论依据和潜在干预策略。
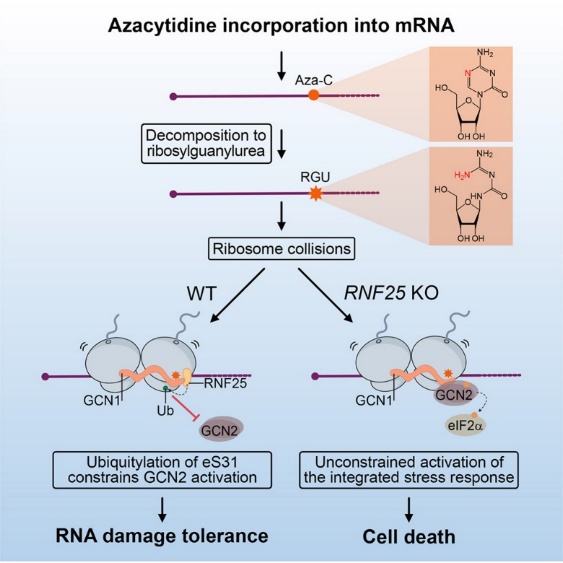
图3:RNF25介导的细胞抵抗阿扎胞苷毒性机制模式图
论文链接://www.cell.com/molecular-cell/fulltext/S1097-2765(26)00138-3
作者简介
赵书博,香港色情片
副教授,香港色情片
“唐敖庆青年学者” 主要研究方向为核酸损伤应答与修复机制及其病理生理学意义。研究成果以第一作者(共同)和通讯作者身份发表在Cell、Molecular Cell、Nucleic Acids Research等国际知名期刊。
【供稿】芦春艳 【编审】李冬 【终审】李东洋